
|

|

|

|

|

|
anterior |
ir a "Índice" |
ir a "Trabajos de biología" |
siguiente |
TEMA 6: LA TRANSFERENCIA DE
INFORMACIÓN
|
CONTENIDO |
|
TEMA 6: LA TRANSFERENCIA DE INFORMACIÓN 1. INTRODUCCIÓN.
El “dogma central” de la Genética Molecular. 2. REPLICACIÓN
DEL ADN. Replicación semiconservadora del ADN:
experimento de Meselson-Stahl.
Replicación del ADN. 3. TRANSCRIPCIÓN: BIOSÍNTESIS DEL ARN. 4. TRADUCCIÓN: BIOSÍNTESIS DE PROTEÍNAS. Descripción y localización
de los ribosomas. La síntesis de proteínas (Síntesis de los aminoacil-ARN-t, iniciación, elongación y terminación).
Diferencias entre Diferencias entre la biosíntesis de polipéptidos en células
eucarióticas y en células procarióticas. Regulación de la síntesis de
proteínas. 5. EL CÓDIGO GENÉTICO. Características: universal y degenerado. |
1. Introducción
En 1953 J.D.
Watson y F.H.C. Crick postularon la estructura de doble hélice del ADN.
Dicha estructura era acorde con la equivalencia molar de bases y con los
diagramas de rayos X característicos del ADN. Pero
además indicaron la existencia de un mecanismo sencillo por medio del cual la
información podía pasar de las células progenitoras a las células hijas.
La hipótesis pronto fue
desarrollada y extendida, hasta llegar a lo que Crick
denominó dogma central de la Genética Molecular: la información genética
fluye del ADN al ARN y de éste a las proteínas. Posteriormente este enunciado
ha sido modificado de la siguiente forma:
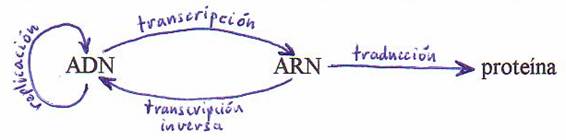
2. Replicación del ADN
a) Replicación semiconservadora del ADN: experimento de Meselson-Stahl
Desde el punto de vista
genético, la característica más sobresaliente de la hipótesis de Watson y Crick acerca de la
estructura en doble hélice del ADN, era que las dos hebras del ADN eran
complementarias, y que la replicación de cada una de ellas da lugar a dos
moléculas de ADN dúplex, cada una de las cuales contiene una hebra del ADN
progenitor. Es lo que denominamos replicación semiconservadora.
Pero existen otras dos posibilidades de replicación por las cuales obtendríamos
dúplex de ADN hijos iguales a los del progenitor: la conservadora y la dispersora:
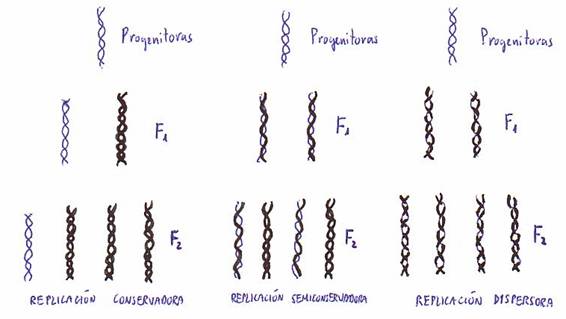
Meselson y Stahl
trabajaron con E. coli y demostraron que su
ADN se replicaba por el mecanismo semiconservador
propuesto por Watson y Crick:
1) Cultivaron E. coli (varias generaciones) en un medio cuya única
fuente de N era NH4Cl marcado con el
isótopo pesado N15.
2) Continuaron el cultivo de
esas E. coli marcadas con N15 en un
medio con N14-NH4Cl normal como única fuente de N
(varias generaciones).
3) Extrajeron ADN de las
muestras y determinaron la densidad de flotación por centrifugación en
gradientes de densidad de CsCl.
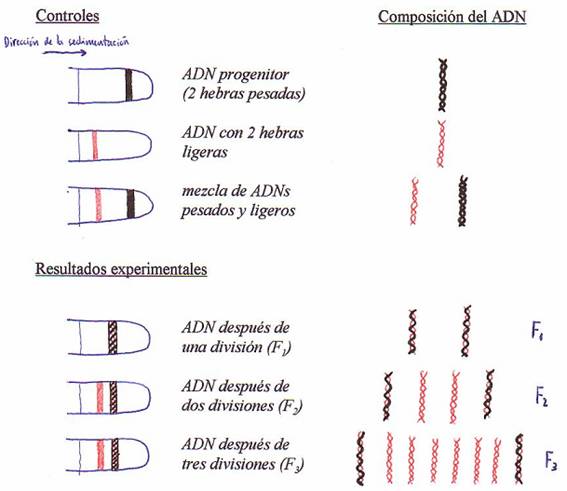
Sólo
encontraron ADN con densidad de flotación media (una hebra pesada y otra
ligera) o con densidad de flotación baja (dos hebras ligeras de nueva síntesi: la replicación era, pues, semiconservadora.
b) Replicación del ADN
Los estudios realizados acerca
de la replicación del ADN se deben al descubrimiento (en 1956, por Arthur Kornberg y cols.) de la enzima ADN-polimerasa
I. La ADN-polimerasa I de E. coli cataliza la síntesis de
los polímeros de ADN a partir de los cuatro desoxirribonucleósidos-5'-trifosfato, en presencia de Mg2+ y con
eliminación de pirofosfato:
dNTP + (dNMP)n W (dNMP)n+1 + PPi
El crecimeinto
de la cadena se realiza en dirección 5' ===> 3'.
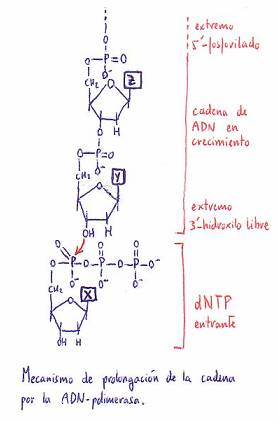
El ADN de doble hebra intacto no
ceba la reacción, a no ser que contenga mellas en alguna de sus dos hebras.
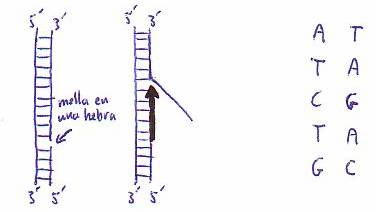
La enzima construye una hebra de
ADN complementaria a la hebra patrón, como se muestra por el análisis de la
composición de bases.
Además, otros análisis han
mostrado que la polaridad de la nueva hebra es opuesta a la de la hebra patrón,
es decir, que se trata de una hebra antiparalela.

La ADN-polimerasa
I presenta además 2 actividades exonucleásicas
(3'==>5' y 5 ==>3'), que ejercen funciones de "corrección de
pruebas", al eliminar nucleótidos no apareados.
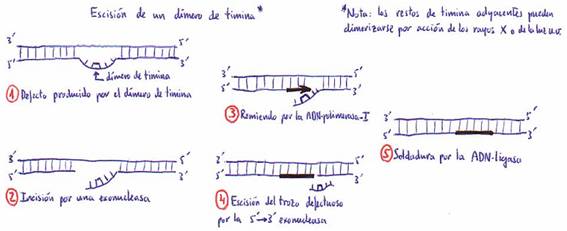
En la síntesis de ADN interviene
además otra enzima: la ADN-ligasa. Esta enzima
repara las mellas que pueden existir en las hebras de ADN. La ADN-ligasa puede unir los extremos de 2 cadenas de ADN si son
los dúplex de una misma hebra complementaria.
Los mutantes deficientes en ADN-polimerasa I condujeron al descubrimiento de las ADN-polimerasas II, III y III*. Ésta, junto con la proteína copolimerasa III*, constituye la forma responsable de la
replicación del ADN, mientras que la ADN-polimerasa I
funciona como auxiliar, así como en la reparación del ADN.
Okazaki encontró que ambas hebras del
ADN se replican formando cortos fragmentos, de hasta 2000 restos nucleotídicos, los cuales se unen por acción de una ADN-ligasa. Esos fragmentos se denominan fragmentos de Okazaki.
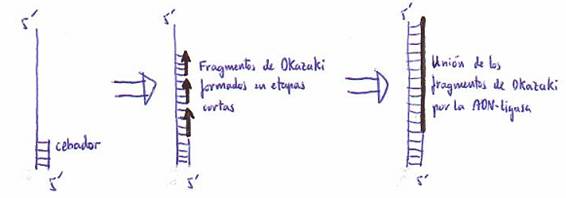
La replicación del ADN requiere
la participación de proteínas desenrolladoras y destorcedoras. Además, dicha replicación necesita ser
cebada por la acción de la ARN-polimerasa-ADN-dirigida,
que fabrica unos cortos tramos de ARN cebadores sobre los que se
construye el ADN; posteriormente, los ARN cebadores son escindidos y
eliminados.
Mientras que en los procariotas los fragmentos de Okazaki
son de 1000 a 2000 nucleótidos, en los eucariotas son
mucho más cortos (de 100 a 150 nucleótidos).
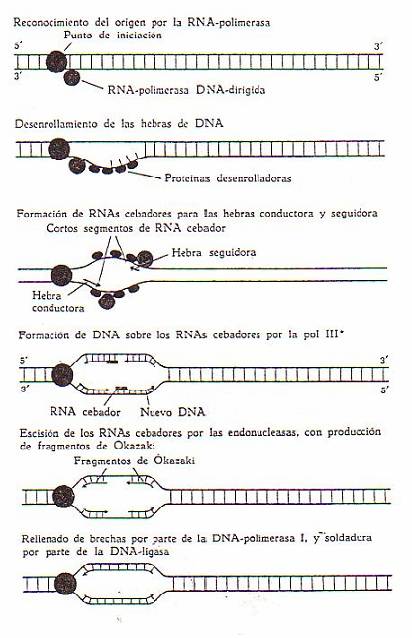
La hipotética secuencia de
etapas en la replicación del ADN quedaría así:
1) Reconocimiento del punto
de iniciación.
2) Desenrollamiento
del ADN.
3) Cebado por el ARN (de
50 a 100 restos) gracias a la acción de una
ARN-polimerasa-ADN-dirigida.
4) Formación de ADN sobre los
ARN cebadores.
5) Eliminación de los ARN
cebadores.
6) Unión de los fragmentos de
ADN: primero, las brechas que quedan entre los fragmentos de Okazaki se rellenan por acción de la ADN-polimerasa
I, y los terminales 5' y 3' se
"sueldan" por acción de la ADN ligasa.
El ADN puede también ser
sintetizado por la ADN-polimerasa-ARN-dirigida
o transcriptasa inversa, presente en algunos
virus de ARN cancerígenos así como en células normales.
3. Transcripción:
biosíntesis del ARN
Los ARN son sintetizados por la ARN-polimerasa-ADN-dirigida a partir de los ribonucleósidos-5'-trifosfato.
La ARN-polimerasa
cataliza la reacción, que se produce en presencia de
Mg2+ y produce pirofosfato:
NTP + (NMP)n ====> (NMP)n+1 + PPi
El funcionamiento de la ARN-polimerasa es similar al de la
ADN-polimerasa, pero no necesita cebador. Desarrolla
el proceso de síntesis en sentido 5' ===> 3'.
Se ha comprobado que in vivo
sólo se transcribe un ahebra de ADN.
La ARN-polimerasa
requiere factores especiales para el reconocimiento del punto de iniciación. El
primer nucleósido-5'-trifosfato
o nucleótido iniciador es siempre el ATP o el GTP y se fija a la polimerasa para formar el complejo de iniciación.
Los ARN-m son modificados por el
acoplamiento de una larga cola de poli A a su extremo
3'.
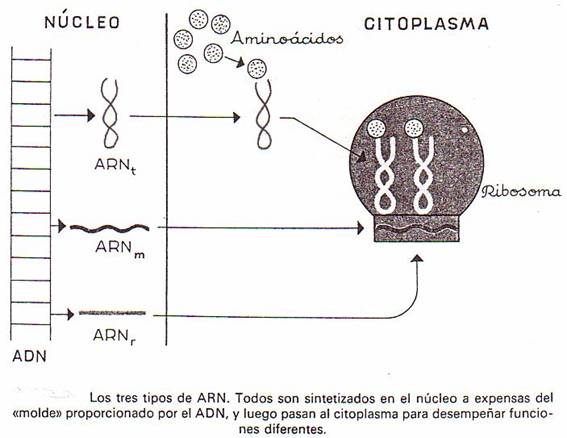
Los ARN-r se generan a partir de
una larga cadena precursora que finalmente es escindida para dar lugar a los
ARN acabados.
A partir de un solo gen pueden
ser transcritas muchas cadenas de ARN simultáneamente.
El aspecto que presentan los genes nucleolares de un huevo de anfibio, que codifican el ARN-r, aparece reflejado en el siguiente dibujo:
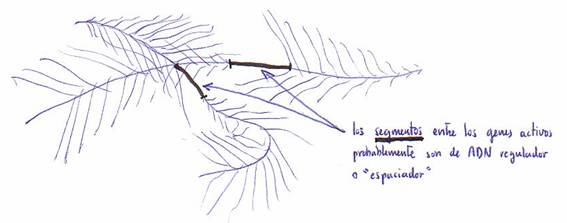
Cada gen experimenta transcripción en ARN-r y forma unas 100 hebras de éste
simultáneamente y a medida que las moléculas de ARN-polimerasa
se deslizan a lo largo del gen.
Por último hay que añadir que
existen unas ARN-polimerasas-ARN-dirigidas,
también conocidas por ARN-replicasas, que se
forman en células bacterianas infectadas por virus-ARN.
La ARN-replicasa
requiere ARN como patrón y no funciona con el ADN. Pero además, en contraste
con las ADN- y las ARN-polimerasas, las ARN-replicasas exhiben especificidad de patrón (la ARN-replicasa inducida por el virus Qβ puede utilizar como
patrón solamente el ARN del propio virus: no replica los ARN de la célula
huésped).
4. Traducción: biosíntesis de
proteínas
a) Descripción y localización
de los ribosomas
Los ribosomas son orgánulos de
muy pequeña dimensión (unos 180 Å en procariotas y
200-220 Å en eucariotas), formados por ribonucleoproteínas, y presentes en todos los tipos de
células ya que son esenciales en la biosíntesis de proteínas.
Están formados por ARN-r y
proteínas (60-65% de ARN-r y 35-40% de proteinas).
Son diferentes los ribosomas de
células procarióticas y los de células eucarióticas. Aunque en ambos casos
están constituidos por 2 subunidades desiguales -una
grande y otra pequeña- que permanecen establemente unidas cuando en el medio
hay una concentración relativamente elevada de Mg2+.
Hay que recordar que los
ribosomas mitocondriales y los cloroplastidiales
se asemejan por sus características a los de procariotas:
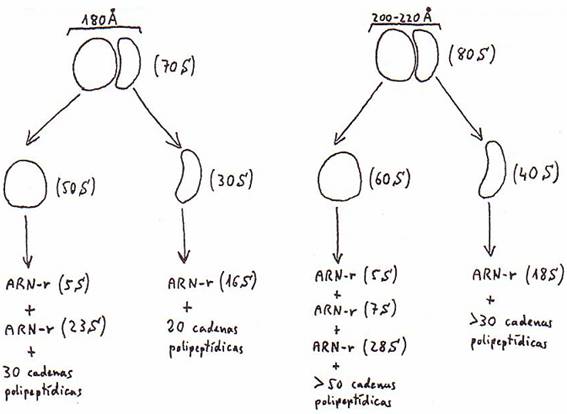
Los ribosomas procarióticos (70
S) pueden encontrarse libres en el citoplasma o asociados en forma de rosarios
llamados polirribosomas o polisomas (constituidos por cierto número de ribosomas unidos
a una única molécula de ARN-m durante la síntesis de proteinas).
Los ribosomas eucarióticos (80
S) pueden encontrarse libres en el citoplasma o como polirribosomas,
igual que los de procariotas. Pero también aparecen
unidos a la superficie del retículo endoplasmático
rugoso, y en el núcleo celular (donde son sintetizados).
Por último, los ribosomas
aparecen en el interior de cloroplastos y de mitocondrias de las células
eucarióticas. Pero estos ribosomas presentan un coeficiente de sedimentación
similar al de los ribosomas procarióticos (70 S).
b) La síntesis de proteínas
Para estudiar el proceso de
biosíntesis proteica, reconocemos 3 etapas: iniciación, prolongación y
terminación.
Previamente a estas 3 etapas se
producirá la síntesis de los aminoacil-ARN-t.
Se sabe que algunas de las
proteínas de los ribosomas tienen una función catalítica. La función del ARN-r
no está todavía clara. Pero parece que el conjunto de ARN-r-proteínas que
constituye los ribosomas actúa como un sistema mecano-químico que podemos
incluir en el mismo tipo de bioestructuras que la actomiosina del músculo y los microtúbulos
de los flagelos eucarióticos.
Estudiaremos el proceso de
traducción en procariotas y señalaremos después las
diferencias con la traducción en eucariotas.
*Síntesis de los aminoacil-ARN-t
Previamente a la síntesis
polipeptídica está la de los aminoacil-ARN-t a partir
de aminoácidos y ARN-t por acción de aminoacil-ARN-t
sintetasas, cada una de las cuales es
estrictamente específica de un aminoácido y de su correspondiente ARN-t. La
reacción que catalizan es:
aminoácido +
ARN-t + ATP
======> aminoacil-ARN-t +
AMP + PPi
La estructura general de los aminoacil ARN-t resultantes es la siguiente:
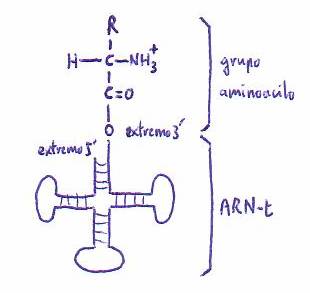
*Iniciación de las cadenas polipeptídicas
La traducción de los codones de ARN-m se desarrolla en sentido 5'==>3'.
Dentro del ribosoma (en la subunidad mayor) se conocen 2 centros: 1) el centro peptidilo (o centro P) y 2) el centro aminoacilo
(o centro A).
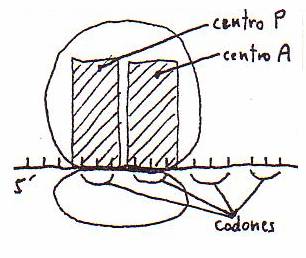
En
procariotas, la síntesis de todas las proteínas
comienza con el aminoácido metionina, codificado por
el codón de iniciación AUG. No entra
como metionil-ARN-t sino como N-formil-metionil-ARN-t.
Durante
la síntesis proteica se da una continua disociación de los ribosomas 70 S en
sus subunidades 50 S y 30 S, y una también continuada
reasociación de las subunidades para dar ribosomas
intactos.
Esto se debe a que los ribosomas
70 S tienen que disociarse para que pueda empezar la síntesis. El ARN-m y el aminoacil-ARN-t no pueden unirse directamente a los
ribosomas 70 S, sino que primero se unen a las subunidades
30 S, las cuales se combinan entonces con las 50 S.
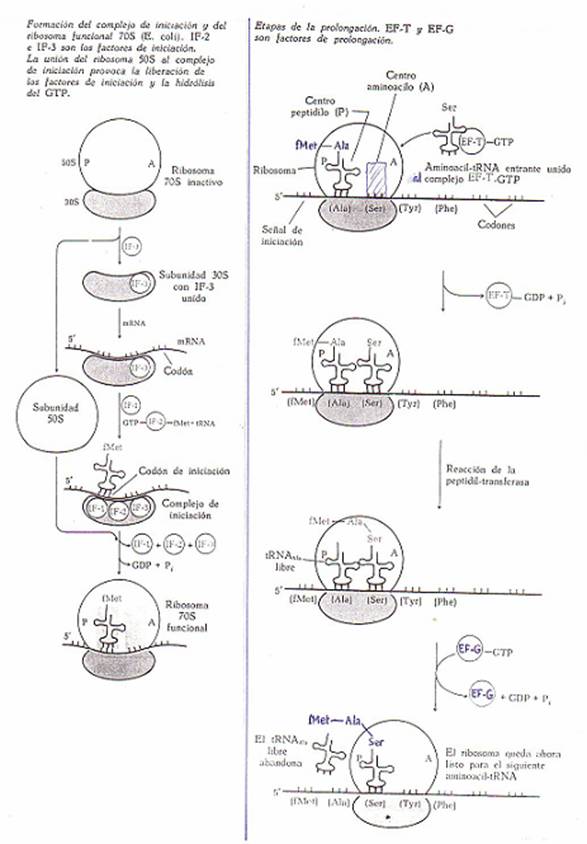
Es un proceso que comprende
múltiples etapas y requiere la participación de 3 proteínas específicas,
denominadas factores de iniciación (IF-1, IF-2 e IF-3, de peso molecular
aproximado: 9000, 65000 y 21000, respectivamente).
En primer lugar la subunidad 30 S forma un complejo con el IF-3, que entonces
se une al ARN-m. A este complejo se le suma una molécula de IF-1.
Entonces el f-Met-ARN-t y GTP se unen al IF-2 y el complejo resultante se
enlaza al anterior (sub. 30 S, IF-3, ARN-m e IF-1), con lo que se forma el
complejo de iniciación.
Después, el complejo de
iniciación se combina con la subunidad 50 S y forma
el ribosoma 70 S funcional. En este proceso se hidroliza el GTP a GDP + Pi, y los 3 factores de iniciación (IF-1, IF-2 e IF-3) se
disocian del ribosoma.
*Prolongación
Tiene 3 etapas:
a) Unión del aminoacil-ARN-t entrante: en la primera etapa se une el aminoacil-ARN-t entrante al centro aminoacilo
(centro A) del complejo ribosómico 70 S completo:
*Combinación del GTP con una proteína
específica: factor de prolongación T (EF-T) que tiene 2 subunidades, una de las cuales se desprende.
*Combinación del complejo EF-T-GTP con el aminoacil-ARN-t.
*Combinación del complejo ternario con el
ribosoma, de forma que el aminoacil-ARN-t se une -por
el centro A- con su anticodón al codón
correspondiente del ARN-m por puentes de H. En este paso el GTP se hidroliza a
GDP + Pi. Sale el complejo EF-T-GDP del ribosoma.
b) Formación del enlace
peptídico:
entre el grupo amino del aminoacil-ARN-t entrante en
la etapa anterior y el carboxílico del f-Met-ARN-t,
se establece un enlace peptídico. Esta reacción es catalizada
por la peptidil transferasa
presente en la subunidad 50 S del ribosoma.
El producto es un dipeptidil-ARN-t unido al centro A, mientras que el ARN-t
descargado o libre permanece unido al centro P. La energía del enlace peptídico
no se obtiene de ATP ni de GTP. Parece que se consigue de la ruptura del enlace
éster de la N-f-Met con su ARN-t.
Un proceso similar sucede en
cada ciclo de la prolongación.
c) Transposición: el ribosoma se traslada al
nuevo codón del ARN-m y simultáneamente cambia el peptidil-ARN-t desde el centro A al centro P.
Este proceso -complejo- de
transposición se verifica según una secuencia de etapas bien definida. Se
requiere una proteina específica denominada factor
de prolongación G (EF-G) y GTP.
1) Se une EF-G a GTP, y el complejo EF-G-GTP
al ribosoma.
2) Se hidroliza el GTP a GDP + Pi y con esa energía se traslada el ribosoma al nuevo codón, y cambia el peptidil-ARN-t
del centro A al centro P.
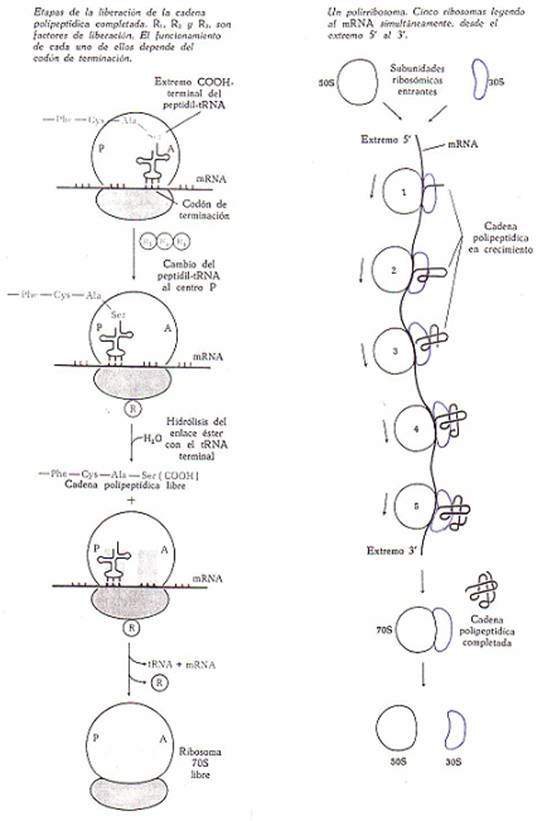
*Terminación de la cadena polipeptídica
La terminación de las cadenas
polipeptídicas está señalizado por uno de los tres codones especiales de terminación en el ARN-m.
Cuando se ha unido ya el último
aminoácido del polipéptido, éste se encuentra todavía unido por el grupo
carboxilo terminal al ARN-t situado en el centro A del ribosoma.
Intervienen entonces 3 proteinas específicas denominadas factores de liberación
(R1, R2 y R3).
a) Los factores se unen al ribosoma
y provocan un desplazamiento del polipeptidil-ARN-t
desde el centro A al centro P.
b) A continuación se hidroliza el
enlace éster con el ARN-t terminal -según parece, por acción de la peptidil transferasa- de forma
que queda la cadena polipeptídica libre.
c) Una vez liberado el polipéptido, el último
ARN-t y el ARN-m abandonan el ribosoma. El ribosoma 70 S libre se puede
disociar en sus subunidades 50 S y 30 S por
intervención de uno de los factores de iniciación específicos y empezar una
nueva síntesis polipeptídica.
c) Diferencias entre la
biosíntesis de polipéptidos en células eucarióticas y en células procarióticas
El aminoácido iniciador en
eucarióticas es metionina (en procarióticas era N-formil-metionina).
En ribosomas eucarióticos los
factores de prolongación son EF1 y EF2 (no EF-TU
y EF-TS de procarióticos).
d) Regulación de la síntesis
de proteínas
Al estudiar el flujo de
información desde el ADN a las proteínas, nos planteamos el modo que tiene la
célula de regular la síntesis proteica de forma que se sinteticen las clases de
proteínas correctas y en el número adecuado de ejemplares de cada una. Así, en
un ser tan elemental como la bacteria E.
coli, que presenta unas 3.000 proteínas
diferentes: 1) al tener cada célula unos 15.000 ribosomas, podemos decir que de
cada una de las 50 ó más proteínas ribosómicas habrá unas 15.000 moléculas; 2) de algunas enzimas de la vía glucolítica pueden encontrarse por lo menos 100.000
ejemplares; 3) de la enzima β-galactosidasa se hallan sólo unos 5
ejemplares por célula. De esta forma, la bacteria tiene el adecuado número de
enzimas para mantener las actividades fundamentales de autogobierno, y
economiza el empleo de aminoácidos para la síntesis de enzimas que utilizará
menos.
En los organismos eucariotas, la regulación de la síntesis de proteínas tiene
otro papel fundamental: constituir el vehículo de diferenciación de las
células, ya que los distintos tipos de células de los organismos superiores poseen
diversas ultraestructuras, distinta composición
molecular y diferentes funciones biológicas (y algo similar sucede con los
tejidos que constituyen).
La biosíntesis proteica se
encuentra regulada, `por lo menos, a dos niveles distintos: el control de transcripción (regulación de la transcripción
de ADN para producir un ARN-m que codifique para una determinada proteína o
conjunto de proteínas); y el control de traducción (regulación de la
iniciación y de la velocidad de síntesis de las cadenas polipeptídicas).
Actualmente se admite la
existencia de dos tipos de enzimas -y con ellos, también de proteínas- que
difieren en su estado natural y en su concentración bajo distintas condiciones
metabólicas: las enzimas constitutivas y las inducibles.
Las enzimas constitutivas
son las que se forman a velocidades constantes y en cantidades también
constantes, independientemente de cuál sea el estado metabólico del organismo.
Forman parte de la maquinaria básica y permanente de la célula. Un ejemplo de
enzimas constitutivas son las enzimas de la vía glucolítica.
Las enzimas inducibles
se encuentran normalmente en cantidades muy pequeñas, pero pueden aumentar su
concentración hasta mil veces o más cuando se hallan en presencia de su
sustrato (particularmente cuando dicho sustrato es la única fuente de C de la
célula). Un ejemplo de enzima inducible es el de la β-galactosidasa:
las células del tipo salvaje de E. coli no
utilizan lactosa si hay glucosa disponible (por eso sólo contienen unas cinco
moléculas de β-galactosidasa, suficientes para hidrolizar la lactosa a
glucosa + galactosa); pero si se ponen esas células en un medio cuya única
fuente de C sea la lactosa, inicialmente no pueden aprovecharla, pero al cabo
de uno o dos minutos reaccionan sintetizando β-galactosidasa en grandes
cantidades, de hasta 5.000 moléculas por célula. Si a continuación las células
inducidas se transfieren a un medio con glucosa pero no lactosa, la síntesis de
β-galactosidasa cesa inmediatamente y la actividad galactosidásica
disminuye rápidamente hasta su bajo nivel normal. La inducción enzimática hace posible la economía del uso de aminoácidos
y de energía disponible: las enzimas inducibles se
sintetizan sólo cuando se necesitan.
A veces una secuencia completa
de enzimas es inducida en grupo (inducción coordinada), o reprimida como grupo
(represión coordinada). Los conjuntos de genes para tales grupos de enzimas se
denominan operones. Cada operón contiene, además de los genes
estructurales de las enzimas cuya síntesis controla, un gen regulador (que
codifica para una proteína represora) y un gen operador. La proteína represora
normalmente está unida al gen operador y evita la transcripción
de los genes estructurales. Pero en presencia del sustrato de la enzima inducible, el sustrato se une a la molécula represora y
libera así al operador, con lo que los genes estructurales quedan disponibles
para la transcripción. Todo esto ha sido estudiado en
el operón lac, que controla la síntesis
de la β-galactosidasa y de otras dos enzimas relacionadas en E. coli.
Aunque el mecanismo explicado
ahora actúa en la transcripción, y así sucede con la
mayoría de los mecanismos de regulación de la expresión genética (y resulta
eficaz, pues la vida media de los ARN-m bacterianos es de unos 2 minutos), se
cree que en ciertas circunstancias también se da una regulación que actúa sobre
la traducción.
La regulación de la expresión
genética en eucariotas es mucho más compleja, ya que:
muestran inducción enzimática en presencia de
sustratos específicos y de ciertas hormonas; intervienen mediadores como el AMP
cíclico y el GMP cíclico; y tienen operones complejos.
5. El código genético
Partiendo únicamente de
consideraciones matemáticas, hace ya mucho tiempo se consideró la posibilidad
de que cada aminoácido estuviera codificado por un pequeño número de
nucleótidos consecutivos de la cadena de ADN. Como los nucleótidos que se
combinan en el ADN son solamente 4 (A, G, C y T), y los aminoácidos proteinogenéticos son 20, se necesitaría más de un
nucleótido para codificar cada aminoácido. Y más de 2, puesto que el número de
variaciones con repetición a las que darían lugar esos nucleótidos tomados de 2
en 2 (es decir, el número de ordenaciones diferentes formadas por 2
nucleótidos) sería sólo 42 = 16. Por eso se concluyó que los
vocablos del código de los aminoácidos eran tripletes de nucleótidos. Esta
conclusión fue confirmada posteriormente mediante experimentos bioquímicos
directos realizados con ribosomas.
El número de tripletes
diferentes posibles es de 43 = 64. Como son 20 los aminoácidos
posibles, el código aminoácido es degenerado: tiene múltiples vocablos
de código para todos los aminoácidos, con excepción del Trp
y la Met. La degeneración reside, generalmente, en la tercera posición de su codón, esto es, en su extremo 3': el nucleótido de esta
posición es mucho menos específico que el primero y que el segundo.
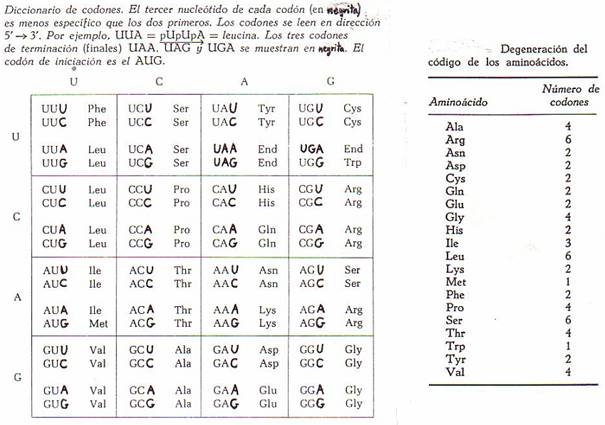
La iniciación de la cadena
empieza en el codón AUG, que codifica a la N-formilmetionina, iniciadora en los procariotas,
y a la metionina iniciadora en los eucariotas.
Los tripletes UAA, UAG y UGA no
codifican a ningún aminoácido, pero constituyen señales de terminación de
cadena: probablemente el UAA sea el terminador de cadena normal.
Los codones
se leen a lo largo de la cadena del ARN-m en sentido 5' ==> 3'.
Actualmente se considera que los
vocablos del código genético que hemos visto antes son biológicamente
universales. El código genético es, casi con toda certeza, universal.
La poca especificidad que hemos
descrito para el tercer nucleótido de los tripletes y la degeneración del
código genético ha dado pie a diversas hipótesis acerca de la evolución del
código genético. Una de esas hipótesis, por ejemplo, plantea la posibilidad de
un código de dobletes inicial seguido de "comas" que con el tiempo
pasarían a ser símbolos del código para permitir así la codificación de más
aminoácidos; esta hipótesis está de acuerdo con la degeneración y la vacilación
de la posición tercera del código de tripletes actual.